不止于概念,干细胞药品已成为现实,这些上市的干细胞药品,经过堪比任何传统化学药物更为严格的临床试验和监管审批流程。它们不是“保健项目”,而是严肃的医疗手段。
目前,全球已有15款间充质干细胞治疗药品获批上市。其中,9款来源于骨髓,3款来源于脐带,2款来源于脂肪,1款来源于脐带血。
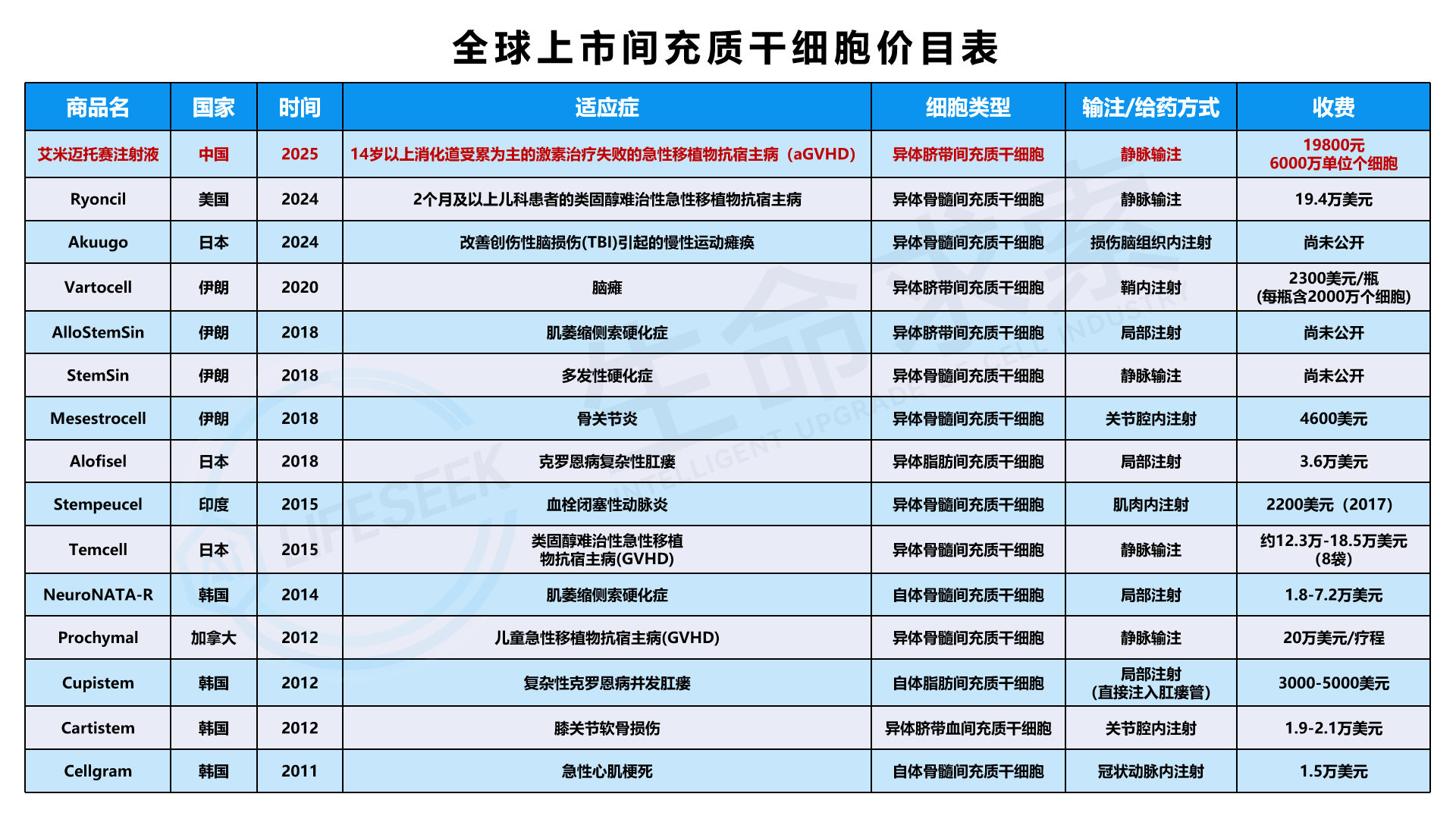
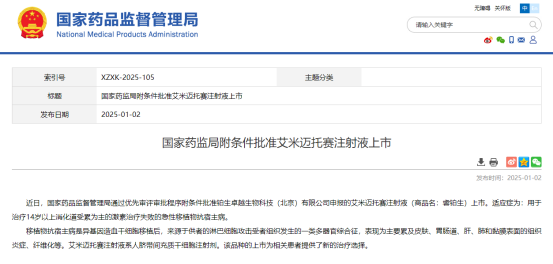
在全球范围内,间充质干细胞药物的研发呈现出蓬勃发展的态势,取得了令人瞩目的阶段性成果。2025年1月2日,国家药品监督管理局通过优先审评审批程序附条件批准艾米迈托赛注射液上市。
截至目前,全球范围内已有至少15款干细胞治疗药品获批上市,它们作为正规的药品,正在中国、美国、日本、韩国等全球多个国家和地区的医院里应用于临床治疗,为数以万计的适应症患者带来了新的希望。
不止于概念,干细胞药品已成为现实,这些上市的干细胞药品,经过堪比任何传统化学药物更为严格的临床试验和监管审批流程。它们不是“保健项目”,而是严肃的医疗手段。
01
盘点全球15款获批上市
干细胞治疗药品
艾米迈托赛注射液
批准国家:中国
批准日期:2025年1月2日
细胞类型:脐带间充质干细胞
适应症:用于治疗14岁以上消化道受累为主的激素治疗失败的急性移植物抗宿主病(aGVHD)
价格:19800元
Ryoncil
批准国家:美国
批准日期:2024年12月18日
细胞类型:同种异体骨髓间充质基质细胞
适应症:用于治疗2个月及以上儿童的类固醇难治性急性移植物抗宿主病(SR-aGVHD)
价格:19.4万美元
剂量:通常8次。每次静脉输注2X10^6MSC/kg,每周两次,连续4周,共输注8次。输注至少间隔3天。
Akuugo
批准国家:日本
批准日期:2024年7月31日(获得条件性和时间限制的批准)
细胞类型:骨髓间充质干细胞
适应症:改善创伤性脑损伤(TBI)引起的慢性运动瘫痪
价格:尚未公开
Vartocell
批准国家:伊朗
批准日期:2020年
细胞类型:脐带间充质干细胞
适应症:脑瘫
价格:1亿伊朗里亚尔(每瓶含2000万个细胞)约2300美元
AlloStemSin
批准国家:伊朗
批准日期:2018年
细胞类型:脐带间充质干细胞
适应症:用于治疗肌萎缩侧索硬化症(ALS)
价格:尚未公开
StemSin
批准国家:伊朗
批准日期:2018年
细胞类型:骨髓间充质干细胞
适应症:用于治疗多发性硬化症
价格:未公开
Mesestrocell
批准国家:伊朗
批准日期:2018年
细胞类型:骨髓间充质干细胞
适应症:用于治疗骨关节炎
价格:2亿伊朗里亚尔(约4600美元)
剂量:关节内注射2x10^7个细胞/单膝;4x10^7个细胞/双膝
Alofisel
批准单位:日本
批准日期:2018年3月23日(欧盟批准);2021年9月(日本批准)
细胞类型:脂肪间充质干细胞
适应症:用于治疗克罗恩病(CD)成人患者的复杂性肛瘘
价格:562万日元/剂(约3.6万美元)
疗程:6ml/瓶,单次治疗剂量1.2x10^8个/24ml (共4瓶)
Stempeucel
批准单位:欧盟、印度
批准日期:2015年6月(欧盟获得孤儿药地位);2020年8月(印度批准);
细胞类型:骨髓间充质干细胞
适应症:用于治疗严重肢体缺血(CLI),包括伯格氏病(Buerger's Disease)和动脉粥样硬化性周围动脉疾病引起的CLI
价格:2200美元(2017年)
Temcell
批准国家:日本
批准日期:2015年9月
细胞类型:骨髓间充质干细胞
适应症:用于治疗急性移植物抗宿主病(GvHD)
价格:868,680日元(约合7,700美元)/袋。一个标准疗程每周2袋,共4周8袋。成年患者通常需要2-3个疗程,即平均需要接受至少16袋或最多24袋。因此总费用约合12.3万美元到18.5万美元。
NeuroNATA-R
批准国家:韩国
批准日期:2014年7月30日
细胞类型:自体骨髓间充质干细胞
适应症:用于治疗肌萎缩侧索硬化症(ALS)和其他运动神经元病
价格:根据患者的体重而有所不同,大约在1.8万至7.2万美元之间
剂量:通常每4周进行两次注射
Prochymal
批准国家:加拿大、新西兰(2016年已从新西兰撤市)
批准日期:2012年5月17日
细胞类型:骨髓间充质干细胞
适应症:用于治疗儿童急性移植物抗宿主病(GvHD)
价格:20万美元/疗程(通常4剂)
Cupistem
批准国家:韩国
批准日期:2012年1月
细胞类型:自体脂肪间充质干细胞
适应症:用于治疗克罗恩病的复杂性肛瘘
价格:约600万韩元(约5000美元/次)
Cartistem
批准国家:韩国
批准日期:2012年1月
细胞类型:脐带血间充质干细胞
适应症:用于治疗退行性关节炎和膝关节软骨损伤
价格:1.9-2.1万美元
CellGram
批准国家:韩国
批准日期:2011年7月1日
细胞类型:自体骨髓间充质干细胞
适应症:用于治疗急性心肌梗死(AMI)
价格:1800万韩元(约合15,000美元),不在医保报销范围内
02
安全的基石
严格的监管与标准
真正让这些上市干细胞药品安全的,是以下几重坚固的保障:
药品级生产标准 (GMP)
上市的干细胞药品必须在符合药品生产质量管理规范的洁净实验室里生产。从供体筛选、细胞采集、培养扩增到储存运输,每一个环节都有极其严格的标准和质控,确保细胞的无菌、无病毒、无致瘤性,且性状稳定均一。
严谨的临床试验
在上市前,这些药品必须经过Ⅰ、Ⅱ、Ⅲ期临床试验,充分验证其在人体内的安全性(是否会产生不良反应)和有效性。(是否对疾病有明确疗效)
权威机构的审批
无论是美国的FDA、中国的NMPA,还是欧洲的EMA,这些监管机构不会对一款有重大安全隐患的产品“开绿灯”。获批上市本身,就是其安全性和有效性在现阶段达到医疗标准的最有力证明。
明确的适应症
每一款上市的干细胞药品都有其明确的适应症。它不是什么“包治百病”的万能神药,而是针对特定疾病、特定人群的精准医疗工具。
LIFE SEEK
写在最后
生命求索旗下医疗机构与阿里健康达成合作,成为艾米迈托赛注射液(中国首款且唯一获批干细胞注射药物)在福建区域的首家合作医疗机构,旗下GMP实验室未来也将成为区域合作实验室。

双方将共同推进该创新药物的可及性与规范化服务,深度融合生命求索的细胞行业优势与阿里健康的数字技术及平台生态,携手探索数字化赋能细胞治疗的新模式,加速革命性疗法惠及患者,为人类健康贡献中国智慧与力量。
以上内容均源于公开发表的文献、学术会议报道或媒体信息,仅供用户了解细胞行业资讯,内容不代表任何药品推广观点或用药建议,亦不能替代医生的独立专业判断,部分图片来自网络,侵删。
关于生命求索
作为国内实现「细胞技术+AI +临床服务+软硬件解决方案+人才培养」全链条赋能的平台型企业,生命求索依托深厚行业积淀的专家团队与自主创新技术体系,提供细胞产、学、研、用整体解决方案。

科研成果转化主要有:细胞智能方舱实验室、TIL细胞、免疫细胞、干细胞、外泌体等。
旗下大模型平台:LIFESEEK 生命求索--国内基于DeepSeek的细胞产业全链条AI大模型平台。
